– سیستم اندازه گیری
در سطح بین المللی، توافقی مبنی بر استفاده از سیستم جایگزینی صورت گرفته که بعضاً به سیستم SI ترجیح داده می شود. در برخی از کشورها سیستم SI به صورت یک پروسه در حال پیاده سازی می باشد.
در این کتابچه سیستم اندازه گیری SI سیستم اصلی مورد استفاده می باشد. اگرچه در بخش های مختلف جامعه تبرید همچنان از سیستم جایگزین استفاده می شود. بنابراین جهت تمرین سیستم جایگزین آن واحدها در داخل پرانتز در صورت نیاز آورده خواهد شد. جدول روبرو سیستم SI و سیستم جایگزین را برای کمیتهای مورد استفاده در این کتابچه نشان می دهد.
| واحد جایگزین | سیستم SI | کمیت |
| h (ساعت) | S (ثانیه) | زمان |
| in(اینچ)؛ft(فوت) | m (متر) | طول |
| lb(پوند) | Kg (کیلوگرم) | جرم |
| ̊c(سلسیوس)؛̊F(فارنهایت) | K (کلوین) | دما |
| Kp(کیلوپوند) | N (نیوتن) | نیرو |
| Bar؛ atm(اتمسفر)؛ mmHg(میلیمتر جیوه)؛ Psi(پوند بر اینچ مربع) | Pa (پاسکال)=N/m2 | فشار |
| Kwh(کیلووات ساعت)؛ cal(کالری)؛ Btu | J (ژول)= Nm | انرژی |
| Cal/h ; btu/h | W (وات)= J/s | توان |
استفاده کاربردی از سیستم اندازه گیری SI با استفاده از پیشوندهایی جهت جلوگیری از نوشتن اعداد خیلی کوچک یا خیلی بزرگ همراه است. قسمتی از پیشوندهای مورد استفاده در جدول زیر نشان داده شده است. مثال: فشار هوای اتمسفر برابرpa 101325 می باشد. نوشتن این عدد با استفاده از جدول زیر می توان به شکل kpa 101.325 باشد.
انتخاب کردن هر کدام از پیشوندهای زیر آزاد می باشد، اما بهترین انتخاب نوشتن اعداد در رنج0.1 تا 9.999 می باشد.
-پیشوندها نباید برای واحدهای ترکیبی استفاده شود، به جز وقتی که kg استفاده می شود. مثال :
2000w/m2k بهتر است به صورت w/m2k 103×2 نوشته شود، نه kw/m2 2.
| نام | پیکو | نانو | میکرو | میلی | کیلو | مگا | گیگا | ترا | پتا |
| پیشوند | p | n | µ | m | K | M | G | T | P |
| ده به توان | 12- | 9- | 6- | 3- | 3 | 6 | 9 | 12 | 15 |
-دما
دما یک مشخصه مرکزی تبرید می باشد. در حقیقت تمام سیستم های تبریدهدفی جز کاهش دمای شیء مانند هوای داخل یک اتاق یا مواد نگهداری شده در آن اتاق را ندارند.
واحد دما در سیستم SI، کلوین (k) یک دمای مطلق است زیرا نقطه مبدأ آن k0 است که پایین ترین دمایی است که در تئوری می توان تعیین کرد. زمانی که با سیستم تبرید کار می کنیم درجه سلسیوس
(̊c درجه سانتیگراد) یکایی است که مورد استفاده عملی قرار می گیرد. سلسیوس یک مقیاس دمای مطلق نیست زیرا نقطه مبدأ آن (̊c 0) با نقطه انجماد آب تعیین شده است.
(برابر با k 15/237)
تنها تفاوت بین کلوین و سلسیوس بین نقطه مبدأ آنهاست. این بدان معنی است که اختلاف دمای ̊1 سانتیگراد دقیقاً برابر است با اختلاف دمای یک کلوین. در قسمت علمی جامعه تبرید اختلاف های دما اغلب از k به جای ̊c استفاده می شود که تداخل بین دما و اختلاف دمایی از روی یکا حذف می شود.
-نیرو و فشار

یکای SI نیرو نیوتن (N) می باشد که در واقع (kg m/s2) است.
مردی که لباس های اسکی پوشیده است می تواند روی تل برفی که عمیق هم هست بایستد، در حالی که اگر او لباس ها و چوب های اسکی را از تن خارج کند درون تل برف فرو خواهد رفت. در مورد اول وزن مرد روی یک سطح زیاد (چوب های اسکی) پخش می شود. در مورد دوم همان وزن فقط در سطح کفش های آن مرد تقسیم می شود که بسیار کمتر از مساحت چوب های اسکی است. تفاوت بین این دو مورد فشاری است که مرد بر سطح برف وارد می کند. فشار به عنوان نیروی وارد شده بر یک مساحت تعریف می شود که به اندازه آن مساحت تقسیم می شود. به عنوان مثال در مورد مرد اسکی باز نیرو ( وزن) ثابت می باشد ولی مساحت ها متفاوت می باشد. در مورد اول مساحت زیاد است و بنابراین فشار کم. در مورد دوم مساحت کم است پس فشار زیاد است.
در تبرید فشار به سیال مورد استفاده به عنوان مبرد مرتبط است؛ وقتی که ماده ای به صورت مایع یا بخار درون یک محفظه نگهداری می شود، بخار نیرویی بر دیواره های آن محفظه وارد می کند. نیروی بخار وارده به سطح داخلی تقسیم بر مساحت آن را فشار مطلق می نامند.
به عنوان یک دلیل علمی میزان فشار بعضاً به عنوان “فشار بالاتر از اتمسفر” نامیده می شود که این یعنی فشار اتمسفر (kpa325/101 =bar 013/1) ازفشار مطلق می کاهد. این فشار بالاتر از فشار اتمسفر را معمولاً فشار گیج می نامند. واحد استفاده شده باید فشار گیج یا فشار مطلق بودن را منعکس کند، به همین دلیل جهت فشار مطلق حرف کوچک یا اندیس (a) و جهت فشار گیج (g) مورد استفاده قرار می گیرد. مثال: فشار مطلق bar(a) 10 تبدیل می شود به
bar(g) (013/-10) که برابر bar(g)9 می باشد.
سایر واحدهای اندازه گیری که هنوز امروزه مورد استفاده قرار می گیرند عبارتند از میلیمتر جیوه (mmHg) و فشار گیج ستون آب (mwg). واحد دوم اغلب در ارتباط با پمپ و ارتفاع ستون آب که آن پمپ می تواند ایجاد کند استفاده می شود.
خلأ (وکیوم) به عنوان فشار مطلق pa0 تعریف می شود، اما از آنجاییکه معمولاً رسیدن به فشار خلأ غیر ممکن است، این اصطلاح عموماً جهت توصیف فشاری بسیار پایین تر از فشار اتمسفر استفاده می شود. مثال: فشار مطلق bar(a)1/0 تبدیل می شود به bar(g) (013/1-1/0) که برابر است با bar(g)9/0- . خلأ همچنین به صورت Torr ( یک Torr برابر است با pa10) و میلی بار(یک هزارم بار) توصیف می شود.
-حرارت، کار، انرژی، توان
حرارت و کار هر دو شکل هایی از انرژی هستند که می توانند بین اجسام منتقل شوند. انتقال حرارت ارتباط بسیار نزدیکی با دما (یا اختلاف دما) موجود بین دو یا چند جسم می باشد. به خودی خود حرارت از جسم با دمای بالاتر به جسم با دمای پایین تر منتقل می شود. گرم شدن آب درون کتری روی اجاق گاز بهترین مثال جهت انتقال حرارت می باشد. صفحه اجاق داغ می شود و حرارت از صفحه به کف کتری و سپس به آب انتقال می یابد. انتقال حرارت به آب سبب بالا رفتن دمای آب می شود. به عبارت دیگر گرم کردن یک شیء همان انتقال انرژی(حرارت) به آن است.
در بسیاری از کاربردهای عملی نیاز است تا دمای یک شیء به جای بالا رفتن کاهش یابد. پس از مثال بالا در میابیم که این اگر شما جسمی دارید با دمای پایین تر از جسمی که می خواهید خنک کنید، با در تماس قرار دادن آن دو انتقال حرارت از جسم مورد نظر به جسم خنک تر رخ می دهد و در نتیجه دمای جسم شما کاهش می یابد. به عبارت دیگر خنک کردن یک شیء یعنی گرفتن انرژی(حرارت) از آن جسم.
مثال انتقال کار مانند استفاده از یک شفت مکانیکی مانند شفتی که موتور الکتریکی یا موتور احتراق را میچرخاند می باشد. اشکال دیگر کار نیز وجود دارد ولی اصلی ترین شکل مورد استفاده در سیستم تبرید استفاده از شفت می باشد.
لازم به یادآوری است که هم حرارت و هم کار اشکال مختلف انرژی هستند. روش های انتقال بین دو شیء متفاوت است اما در یک فرآیند، خروجی فرایند برآیند انتقال حرارت و انتقال کار اندازه گیری شده می باشد.

واحد اندازه گیری حرارت، کار و انرژی در سیستم SI، ژول(J) می باشد. انرژی موردنیاز جهت افزایش دمای یک کیلوگرم آب از 15 درجه سانتیگراد به 16 درجه سانتیگراد KJ 187/4 می باشد. این KJ187/4 می تواند به عنوان کار یا حرارت منتقل شود، اما حرارت راه حل کاربردی در این مورد می باشد.
در اینجا تفاوت هایی در مورد اینکه چقدر انرژی موردنیاز است برای افزایش دمای مواد مختلف به میزان 1 کلوین وجود دارد. برای یک کیلوگرم آهن خالص KJ 447/0 انرژی نیاز است در حالی که جهت یک کیلوگرم هوای اتمسفر KJ 1 مورد نیاز است. خاصیتی که بین هوا و آهن متفاوت است و سبب افزایش دما می باشد را “ظرفیت گرمای ویژه” می نامند که به عنوان انرژی موردنیاز جهت افزایش دمای یک کلوین از یک کیلوگرم هر ماده تعریف می شود. یکای ظرفیت گرمای ویژه J/Kg K می باشد.
نرخ انتقال انرژی را توان می نامند. واحد توان در سیستم SI، واتW می باشد. مثال: اگر در هر ثانیه 10 ژول انرژی منتقل شود، نرخ انتقال انرژی J/S 10 یا همان W10 می باشد. در سیستم SI واحد توان مشابه واحد انتقال حرارت و کار می باشد. در سیستم های دیگر واحد انتقال حرارت و کار ممکن است متفاوت باشد.
-مواد و تغییر فاز
تمام مواد می توانند به صورت سه فاز مایع، جامد و گاز ظاهر شوند. آب یک مثال طبیعی می باشد که ما هرروز به صورت هر سه فاز از آن استفاده می کنیم. در مورد آب هریک از سه فاز نام اختصاصی دارند که اگر به عنوان یک ماده هر کدام را در نظر بگیریم کمی پیچیده می شود. به فاز جامد آن یخ، مایع را آب و به فاز گاز آن بخار می گوییم. چیزی که در این فازها معمول است ملکول های آب بدون تغییر باقی می مانند، این بدان معنی است که یخ، آب و بخار همگی فرمول شیمیایی مشابه H2O را دارند. زمانی که یک ماده از حالت جامد به مایع تبدیل می کنیم به این عملیات ذوب شدن می گویند و فرآیند تبدیل مایع به بخار را جوش آمدن (تبخیر) می نامند. وقتی که از جهت دیگر این فرآیندها را بررسی کنیم فرآیند تبدیل گاز به مایع را میعان (تقطیر) و تبدیل مایع به جامد را انجماد می نامند.

در فشار ثابت، فرآیند تغییر فاز نقش بسیار مهمی را ایفا می کند. زمانی که یخ در فشار 1 بار گرم می شود دمای آن شروع به بالا رفتن می کند. در حین فرآیند ذوب، درجه حرارت یخ تغییری نمی کند؛ در این حالت تمام انرژی وارد بر مخلوط یخ و آب صرف ذوب شدن یخ می شود و نه افزایش آب. تنها در زمانی انرژی وارده سبب بالا رفتن دمای آب می شود که یخ به طور کامل ذوب شده باشد. مشابه چنین رفتاری را می توان در زمان حرارت دادن به آب درون کتری مشاهده نمود. دمای آب تا زمانی که به دمای 100 درجه سلسیوس برسد بالا می رود و سپس تبخیر آغاز می شود. در حین فرآیند تبخیر دمای آب در 100c̊ باقی می ماند. زمانی که آب به طور کامل تبخیر شد دمای بخار آب باقی مانده در ظرف شروع به افزایش می کند. دما و فشار یک ماده در یک زمان، هرچند آن ماده در یکی از فازهای مایع، جامد و گاز و یا حتی ترکیبی از دو یا هر سه فاز باشد معلوم است. در محیط پیرامون ما آهن به شکل جامد ظاهر می شود، آب در فازهای مایع و گاز وهوا در فاز گاز نمایان می باشد.

مواد مختلف نقطه ذوب و جوش متفاوتی دارند. بطور مثال طلا در 1064c̊ ذوب می شود، شکلات در 26c̊ و اغلب مبردها در دمایی حدود 100c̊- ذوب می شود! برای ماده ای که در زمان یکسان در دو فاز موجود است یا اینکه در حال تغییر فاز می باشد، دما و فشار آن ماده به هم وابسته است. اگر دو فاز در یک محفظه بسته باشند و آن دو فاز در حالت تعادل دمایی باشند، به آن شرایط اشباع می گویند. اگر دمای مخلوط دو فاز افزایش یابد مطمئناً فشار نیز افزایش خواهد یافت. ارتباط بین فشار و دما در حالت اشباع(مایع و گاز) را اصطلاحاً منحنی فشار بخار می نامند. یکی از استفاده های منحنی فشار بخار تعیین دما یا فشار اشباع می باشد.
–گرمای نهان
با بازگشت به فرآیند ذوب شدن یخ به نکته مهمی برمی خوریم و آن این است که باید به این نکته توجه کرد که میزان انرژی مورد نیاز جهت ذوب کردن 1 کیلوگرم یخ بسیار بیشتر از انرژی موردنیاز جهت بالا بردن بالا بردن دمای 1 کیلوگرم آب به میزان 1 کلوین می باشد. دربخش های ظرفیت گرمای ویژه آب 4.187 kj/kg.k ذکرشده بود. انرژی مورد نیاز جهت ذوب شدن یک کیلوگرم یخ معادل kj335 می باشد. همین میزان انرژی که یک کیلوگرم یخ را ذوب کرد می تواند دمای یک کیلوگرم آب را به میزان k80 افزایش دهد. (335kj/4.187 kj)
وقتی که به فرآیند تبخیر آب مینگریم، در مییابیم که انرژی مورد نیاز جهت تبخیر 1 کیلوگرم آب برابر 2501 کیلوگرم است. همین میزان انرژی که می تواند 1 کیلوگرم آب را تبخیر کند، میتواند دمای نه تنها 1 کیلوگرم، بلکه 6 کیلوگرم آب را به میزان 100 کلوین افزایش دهد.
این مثالها نشان میدهد که انتقال انرژی مربوط به فرآیند تغییر فازها قابل توجه است. به همین دلیل است که از یخ برای خنک کردن استفاده میکنند؛ انرژی بسیار زیادی نیاز است تا یخ ذوب شودو در تمام این مدت دمای آن 0 درجه سانتیکراد باقی میماند.

اثر خنک کردن در سیستمهای تبرید بر پایه استفاده و کنترل فرآیند تبخیر میباشد. هنگامی که مبرد تبخیر میشود انرژی (حرارت) زیادی را از محیط اطرافش جذب میکند و با در ارتباط قرار دادن یک جسم با حرارت بالا با یک مبرد میتوان دمای آن جسم را کاهش داد.
-سوپرهیت
در واژه شناسی تبرید، سوپرهیت یک عبارت بسیار مهم است؛ اما متآسفانه در راههای متفاوتی استفاده میشود. سوپرهیت میتواند به عنوان فرآیند افزایش دمای یک مبرد پس از تبخیر در شرایط اشباع معرفی گردد. همچنین سوپرهیت میتواند رای توصیف یا اندازهگیری شرایط نهایی قبل از فرآیند فوق استفاده شود. میزان کمی سوپرهیت را میتوانیم به عنوان اختلاف دمای بین دمایی که یک ترمومتر اندازهگیری میکند و دمای اشباع متناسب با فشاری که از روی گیج میخوانیم معرفی کنیم. بنابراین سوپرهیت نمیتواند یک کمیت مستقل باشد و با اندازه گیری یک دما به دست آید؛ بدین منظورداشتن دمای اشباع متناسب با فشار خوانده شده از روی گیج (فشار اشباع) نیز مورد نیاز است.
وقتی سوپرهیت اندازهگیری میشود باید به عنوان اختلاف دما اندازهگیری شود؛ بنابراین بهتر است که در واحد کلوین (K) بیان گردد؛ چون اگر به درجه سانتیگراد (˚c) بیان گردد احتمال بروز خطا بین دمای اندازهگیری شده و میزان سوپرهیت وجود دارد.
فرآیند تبخیر در سیکل تبرید یکی از فرآیندهایی است که از سوپرهیت در آن استفاده میشود. در مطالب بعدی در این مورد بیشتر توضیح داده خواهد شد.
–نمودارهای مبرد
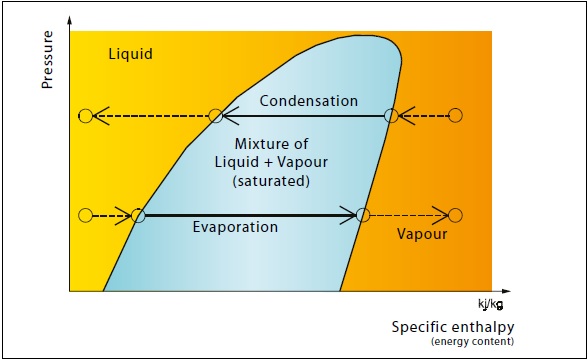
ویژگیهای یک مبرد را میتوان در یک نمودار با استفاده از مشخصات و خواص اولیه که معمولا محتوای انرژی و فشار هستند نشان داد. محتوی انرژی با خاصیت ترمودینامیکی به نام آنتالپی معرفی میشود که با تغییر انرژی در واحد جرم از یک مبرد که تحت فرآیندهای یک سیکل تبرید میباشند تعیین میشوند. به عنوان مثال یک نمودار بر پایه آنتالپی (محور افقی) و فشار (محور عمودی) که به نمودار P-h معروف است در ذیل نشان داده شده است. اندازه کاربردی محور عمودی جهت فشار بسیار بزرگ خواهد بود به همین دلیل در این نمودار از مقیاس لگاریتمی جهت نمایش فشار استفاده میشود. در نمودار ذیل ملاحظه فرمائید که این نمودار سه منطقه فازی مایع، گاز و دوفازی (مخلوط مایع و گاز) را نشان میدهد. بخش مایع در سمت چپ (با میزان انرژی کمتر) و بخش گاز در سمت راست (با میزان انرژی بیشتر) قرار دارند. در بین این دو، ناحیهی دو فازی میباشد. این ناحیه با یک نمودار محصور شده است که به این منحنی، منحنی اشباع میگویند. فرآیندهای تبخیر و تقطیر در شکل ذیل نمایش داده شده است. ایدهی استفاده از نمودار بدین جهت شکل گرفت که این نمودار ارائه فرآیندهای سیکل تبرید را به صورتی که آنالیز و ارزیابی این فرآیندها سادهتر شود را ممکن میسازد. با ستفاده از نمودار میتوانیم شرایط عملکرد سیستم (دما و فشار) را تعیین میکنیم و با یک محاسبه ساده میتوانیم ظرفیت برودتی را داشته باشیم. نمودارها همچنان به عنوان ابزار اصلی آنالیز سیستم برودتی به حساب میآیند. اگرچه تعداد زیادی نرمافزار های محاسباتی که میتواند همین آنالیزها را با سرعت و جزئیات بیشتر در دسترس است.

دیدگاه شما